Автор:
Lewis Jackson
Дата Створення:
12 Травень 2021
Дата Оновлення:
1 Липня 2024

Зміст
Визначити кількість нейтронів в атомі досить просто, навіть не потрібно робити ніяких експериментів. Щоб розрахувати кількість нейтронів у нормальному атомі чи ізотопі, вам просто потрібно підготувати періодичну таблицю та дотримуватися інструкцій.
Кроки
Метод 1 із 2: Знайдіть кількість нейтронів у нормальному атомі
Визначте положення елемента на таблиці Менделєєва. Наприклад, ми знайдемо елемент осмію (Os) у шостому рядку зверху.
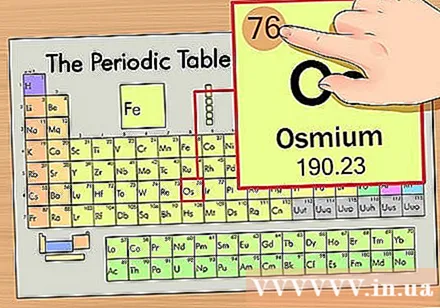
Знайдіть атомний номер елемента. Це найбільш помітне число, яке проходить кожним елементом і знаходиться вище простого символу (на дошці, яку ми використовуємо, немає інших чисел). Атомне число - це кількість протонів в одному атомі цього елемента. Os - це число 76, що означає, що в атомі осмію знаходиться 76 протонів.- Кількість протонів ніколи не змінюється в елементі; це, по суті, визначальна характеристика елемента.
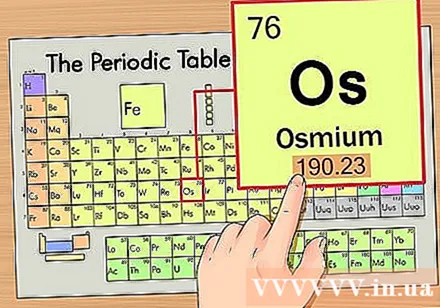
Знайдіть атомну вагу елемента. Це число зазвичай знаходиться під простим символом. Зверніть увагу, що періодична таблиця в цьому прикладі має лише атомний номер і не має атомної ваги. Не всі періодичні таблиці. Атом має осмій 190,23.
Округліть атомну масу до найближчого цілого числа, щоб отримати атомну масу. Наприклад, 190,23 буде округлено до 190, отже атомна маса осмію дорівнює 190.- Атомна вага - це середнє значення ізотопів одного і того ж хімічного елемента, саме тому воно, як правило, не є цілим числом.
Від атомної маси відніміть атомне число. Оскільки більша частина атомної маси - це маса протонів і нейтронів, віднімаючи кількість протонів з атомної маси (тобто атомний номер), ви отримаєте рахувати отримати кількість нейтронів в атомі. Число після десяткової коми представляє дуже малу масу електронів в атомі. У цьому прикладі ми маємо: 190 (масовий атом) - 76 (кількість протонів) = 114 (кількість нейтронів).
Запам’ятайте рецепт. Щоб знайти кількість нейтронів, ми просто застосовуємо таку формулу: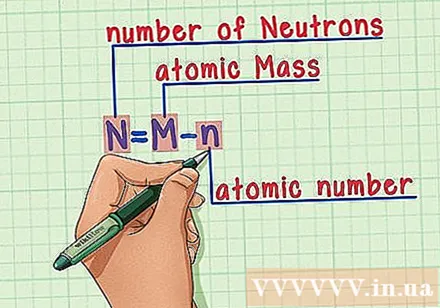
- N = M - n
- N = кількість нейтронів
- М = атомна маса
- n = атомний номер
- N = M - n
Метод 2 із 2: Знайдіть кількість нейтронів в ізотопі
Визначте положення елемента на таблиці Менделєєва. Візьмемо для прикладу елемент ізотоп вуглець-14. Оскільки ізотопною формою вуглецю-14 є просто вуглець (С), шукайте вуглець у періодичній системі (другий рядок зверху).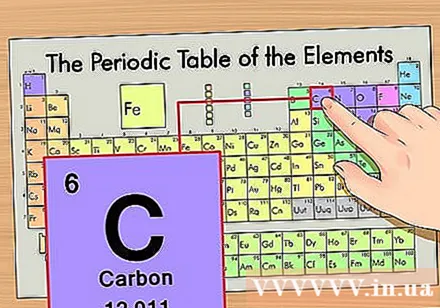
Знайдіть атомний номер елемента. Це найбільш помітне число, яке проходить кожним елементом і знаходиться вище простого символу (на дошці, яку ми використовуємо, немає інших чисел). Атомне число - це кількість протонів в одному атомі цього елемента. С - число 6, що означає, що в атомі вуглецю знаходиться 6 протонів.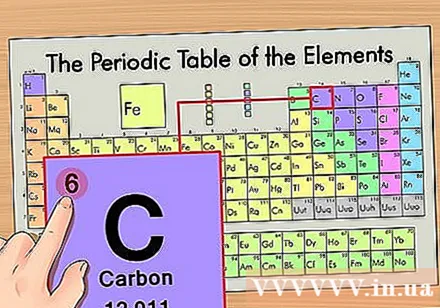
Знайдіть атомну масу. З ізотопами це надзвичайно просто, оскільки вони названі на честь атомної маси. Наприклад, вуглець-14 матиме атомну масу 14. Після того, як ви знайдете атомну масу ізотопу, решта етапів пошуку числа нейтронів будуть такими ж, як у звичайного атома.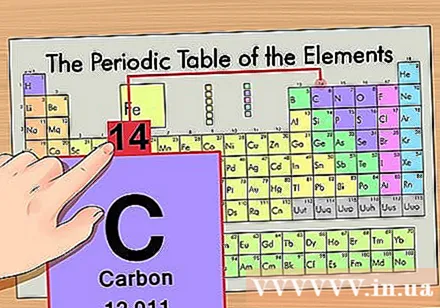
Від атомної маси відніміть атомне число. Оскільки більша частина атомної маси - це маса протонів і нейтронів, віднімаючи кількість протонів з атомної маси (тобто атомний номер), ви отримаєте рахувати отримати кількість нейтронів в атомі. Число після десяткової коми представляє дуже малу масу електронів в атомі. У цьому прикладі ми маємо: 14 (масовий атом) - 6 (кількість протонів) = 8 (кількість нейтронів).
Запам’ятайте рецепт. Щоб знайти кількість нейтронів, застосуємо таку формулу: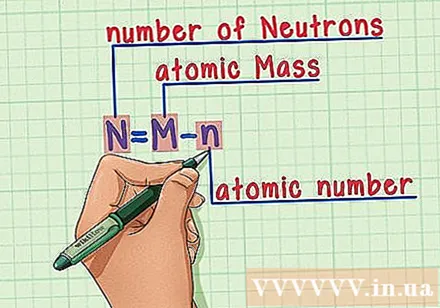
- N = M - n
- N = кількість нейтронів
- М = атомна маса
- n = атомний номер
- N = M - n
Порада
- Маса елемента - це значною мірою маса протонів і нейтронів, тоді як маси електронів та інших елементів незначні (близькі до нуля). Оскільки маса протона приблизно дорівнює масі нейтрона, а атомний номер представляє кількість протонів, нам потрібно лише відняти кількість протонів із загальної маси.
- Якщо ви не пам’ятаєте значення чисел у періодичній системі, пам’ятайте, що періодична система, як правило, побудована на атомних числах (тобто кількості протонів), починаючи з 1 (водень) і збільшуючи одну одиницю від зліва направо, закінчуючись 118 (унуноктій). Оскільки кількість протонів є ідентифікаційною ознакою кожного атома, це найпростіша властивість, за якою розташовані елементи. (Наприклад, атом з 2 протонами - це завжди гелій, як і атом з 79 протонами - це завжди золото.)
Джерела та цитати
- Інтерактивна періодична система