Автор:
Christy White
Дата Створення:
8 Травень 2021
Дата Оновлення:
1 Липня 2024

Зміст
- Крок
- Метод 1 з 3: Частина перша: Розуміння електронних оболонок
- Метод 2 з 3: Частина друга: Пошук валентних електронів у металах, крім перехідних металів
- Метод 3 з 3: Частина третя: Пошук валентних електронів у перехідних металах
- Поради
- Потреби
Валентні електрони лежать у зовнішній оболонці елемента. Кількість валентних електронів в атомі визначає тип хімічного зв’язку, який може утворювати цей елемент. Найкращий спосіб дізнатись кількість валентних електронів - використовувати періодичну таблицю елементів.
Крок
Метод 1 з 3: Частина перша: Розуміння електронних оболонок
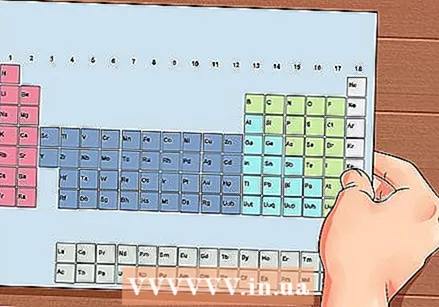 Періодична система елементів. Це таблиця з кольоровими кодами, де в кожній комірці відображається елемент із атомним номером та 1-3 буквами як символ.
Періодична система елементів. Це таблиця з кольоровими кодами, де в кожній комірці відображається елемент із атомним номером та 1-3 буквами як символ. 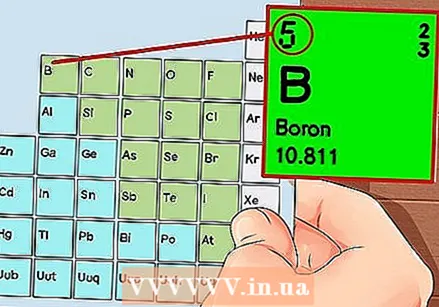 Знайдіть атомний номер елемента. Атомний номер знаходиться вище або поруч із символом елемента. Наприклад: Бор (В) має атомний номер 5, що означає, що він має 5 протонів і 5 електронів.
Знайдіть атомний номер елемента. Атомний номер знаходиться вище або поруч із символом елемента. Наприклад: Бор (В) має атомний номер 5, що означає, що він має 5 протонів і 5 електронів. 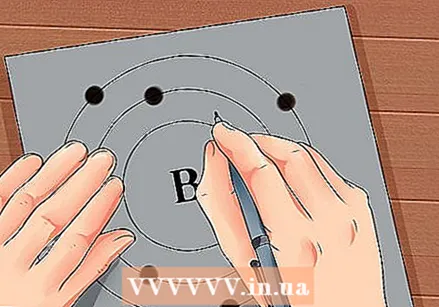 Намалюйте просте зображення атома і розмістіть електрони на орбіті навколо ядра. Ці роботи також називають оболонками або енергетичними рівнями. Максимальна кількість електронів, які можуть знаходитися в одній оболонці, фіксована, і оболонки заповнюються від внутрішньої до зовнішньої орбіти.
Намалюйте просте зображення атома і розмістіть електрони на орбіті навколо ядра. Ці роботи також називають оболонками або енергетичними рівнями. Максимальна кількість електронів, які можуть знаходитися в одній оболонці, фіксована, і оболонки заповнюються від внутрішньої до зовнішньої орбіти. - K Оболонка (внутрішня): максимум 2 електрони.
- L Оболонка: максимум 8 електронів.
- М оболонка: максимум 18 електронів.
- N Оболонка: максимум 32 електрони.
- O Оболонка: максимум 50 електронів.
- P Оболонка (зовнішня): максимум 72 електрони.
 Знайдіть кількість електронів у зовнішній оболонці. Це валентні електрони.
Знайдіть кількість електронів у зовнішній оболонці. Це валентні електрони. - Коли валентна оболонка заповнена, елемент стабільний.
- Якщо валентна оболонка не повна, тоді елемент реактивний, що означає, що він може хімічно зв’язуватися з атомом іншого елемента. Кожен атом ділиться своїми валентними електронами, намагаючись наповнити валентну оболонку.
Метод 2 з 3: Частина друга: Пошук валентних електронів у металах, крім перехідних металів
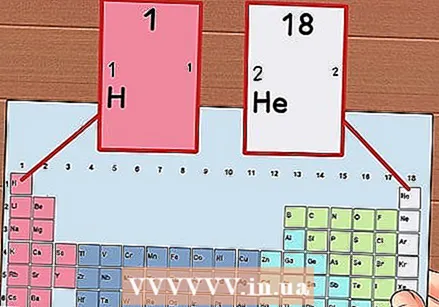 Нумеруйте кожен стовпець періодичної таблиці від 1 до 18. Водень (H) знаходиться у верхній частині колони 1, а гелій (He) - у верхній частині колони 18. Це різні групи елементів.
Нумеруйте кожен стовпець періодичної таблиці від 1 до 18. Водень (H) знаходиться у верхній частині колони 1, а гелій (He) - у верхній частині колони 18. Це різні групи елементів. 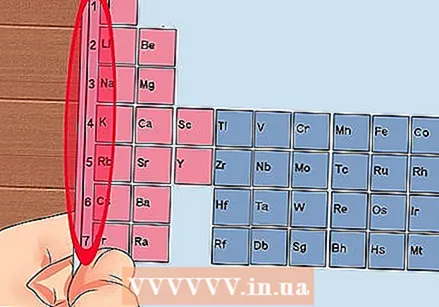 Дайте кожному рядку число від 1 до 7. Це періоди елементів, і вони відповідають кількості оболонок або енергетичних рівнів атома.
Дайте кожному рядку число від 1 до 7. Це періоди елементів, і вони відповідають кількості оболонок або енергетичних рівнів атома. - Водень (H) і гелій (He) мають по 1 оболонці, тоді як у Francium (Fr) - 7.
- Лантаніди та актиноїди згруповані та перелічені нижче основної таблиці. Всі лантаніди належать до періоду 6, групи 3, а всі актиноїди належать до періоду 7, групи 3.
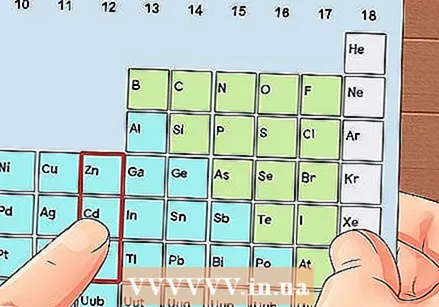 Знайдіть елемент, який не є перехідним металом. Перехідні метали знаходяться в групах з 3 по 12. Номери груп інших металів вказують на кількість валентних електронів.
Знайдіть елемент, який не є перехідним металом. Перехідні метали знаходяться в групах з 3 по 12. Номери груп інших металів вказують на кількість валентних електронів. - Група 1: 1 валентний електрон
- Група 2: 2 валентні електрони
- Група 13: 3 валентні електрони
- Група 14: 4 валентні електрони
- Група 15: 5 валентних електронів
- Група 16: 6 валентних електронів
- Група 17: 7 валентних електронів
- Група 18: 8 валентних електронів - крім гелію, який має 2
Метод 3 з 3: Частина третя: Пошук валентних електронів у перехідних металах
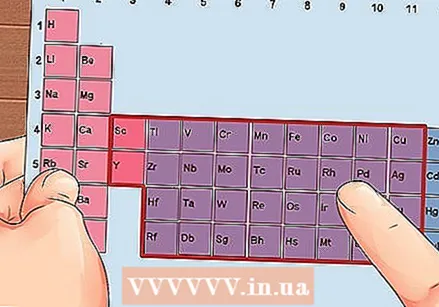 Знайдіть елемент з груп 3 - 12, перехідні метали.
Знайдіть елемент з груп 3 - 12, перехідні метали. Визначте кількість валентних електронів на основі числа групи. Цим групам відповідає можлива кількість валентних електронів.
Визначте кількість валентних електронів на основі числа групи. Цим групам відповідає можлива кількість валентних електронів. - Група 3: 3 валентні електрони
- Група 4: 2 - 4 валентні електрони
- Група 5: 2 - 5 валентних електронів
- 6 група: від 2 до 6 валентних електронів
- Група 7: 2 - 7 валентних електронів
- Група 8: 2 або 3 валентні електрони
- Група 9: 2 або 3 валентні електрони
- Група 10: 2 або 3 валентні електрони
- Група 11: 1 або 2 валентні електрони
- Група 12: 2 валентні електрони
Поради
- Перехідні метали можуть мати валентні оболонки, які не є повністю заповненими. Визначення точної кількості валентних електронів у перехідних металах вимагає певних принципів квантової теорії, які виходять за рамки даної роботи.
Потреби
- Періодична система елементів
- Олівець
- Папір



