Автор:
Eric Farmer
Дата Створення:
10 Березень 2021
Дата Оновлення:
1 Липня 2024

Зміст
- кроки
- Метод 1 з 2: Визначення числа нейтронів в атомах (НЕ ізотопи)
- Метод 2 з 2: Визначення числа нейтронів в изотопах
- Поради
В атомах одного і того ж елемента число протонів незмінно, в той час як число нейтронів може змінюватися.Знаючи, скільки нейтронів міститься в конкретному атомі, ви зможете визначити, чи є він звичайним атомом або ізотопом, який буде мати меншу або більшу кількість нейтронів. Визначити кількість нейтронів в атомі - досить просто. Все, що вам потрібно зробити для розрахунку кількості нейтронів в атомі або ізотопі, - це слідувати нашим інструкціям і тримати під рукою періодичну таблицю.
кроки
Метод 1 з 2: Визначення числа нейтронів в атомах (НЕ ізотопи)
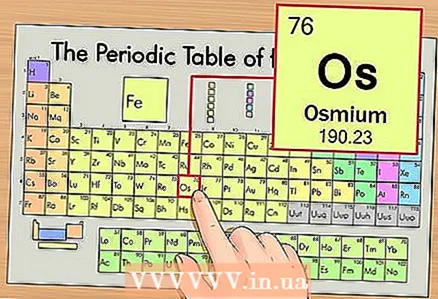 1 Знайдіть елемент в періодичній таблиці. Для прикладу ми будемо розглядати осмій (Os), який знаходиться в шостому періоді (шостий ряд зверху).
1 Знайдіть елемент в періодичній таблиці. Для прикладу ми будемо розглядати осмій (Os), який знаходиться в шостому періоді (шостий ряд зверху).  2 Знайдіть атомний номер елемента. Це, як правило, найбільш помітне число в комірці елемента і зазвичай знаходиться над його символом (в варіанті періодичної системи, яку ми використовуємо в нашому прикладі, інших номерів і немає). Атомний номер - це кількість протонів в одному атомі цього елементу. Для осмію це число 76, тобто в одному атомі осмію міститься 76 протонів.
2 Знайдіть атомний номер елемента. Це, як правило, найбільш помітне число в комірці елемента і зазвичай знаходиться над його символом (в варіанті періодичної системи, яку ми використовуємо в нашому прикладі, інших номерів і немає). Атомний номер - це кількість протонів в одному атомі цього елементу. Для осмію це число 76, тобто в одному атомі осмію міститься 76 протонів. - Число протонів незмінно, саме воно і робить елемент елементом.
 3 Знайдіть атомну масу елемента. Це число зазвичай знаходиться під символом елемента. Зверніть увагу, що у варіанті періодичної системи в нашому прикладі атомна маса не приведена (це не завжди так, в багатьох варіантах періодичної системи атомна маса вказана). Атомна маса осмію - 190,23.
3 Знайдіть атомну масу елемента. Це число зазвичай знаходиться під символом елемента. Зверніть увагу, що у варіанті періодичної системи в нашому прикладі атомна маса не приведена (це не завжди так, в багатьох варіантах періодичної системи атомна маса вказана). Атомна маса осмію - 190,23.  4 Округлите атомну масу до найближчого цілого числа. У нашому прикладі 190,23 округляється до 190.
4 Округлите атомну масу до найближчого цілого числа. У нашому прикладі 190,23 округляється до 190. - Атомна маса - середнє число ізотопів конкретного елемента, зазвичай вона не виражається цілим числом.
 5 Відніміть атомний номер з атомної маси. Оскільки абсолютна частина атомної маси припадає на протони і нейтрони, віднімання числа протонів (тобто атомного номера, який дорівнює числу протонів) з атомної маси дає число нейтронів в атомі. Цифри після десяткової коми ставляться до дуже малої маси електронів в атомі. У нашому прикладі: 190 (атомна вага) - 76 (число протонів) = 114 (число нейтронів).
5 Відніміть атомний номер з атомної маси. Оскільки абсолютна частина атомної маси припадає на протони і нейтрони, віднімання числа протонів (тобто атомного номера, який дорівнює числу протонів) з атомної маси дає число нейтронів в атомі. Цифри після десяткової коми ставляться до дуже малої маси електронів в атомі. У нашому прикладі: 190 (атомна вага) - 76 (число протонів) = 114 (число нейтронів). 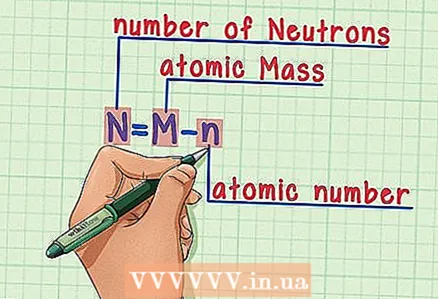 6 Запам'ятайте формулу. Щоб знайти число нейтронів в майбутньому, просто використовуйте цю формулу:
6 Запам'ятайте формулу. Щоб знайти число нейтронів в майбутньому, просто використовуйте цю формулу: - N = M - n
- N = кількість нейтронів
- M = атомна маса
- n = атомний номер
- N = M - n
Метод 2 з 2: Визначення числа нейтронів в изотопах
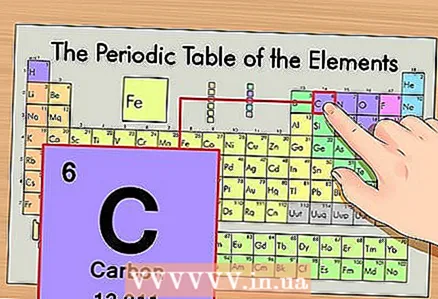 1 Знайдіть елемент в періодичній таблиці. Як приклад ми будемо розглядати ізотоп вуглецю 14С. Оскільки неізотопних вуглець 14С є просто вуглець С, знайдіть вуглець в періодичній таблиці (другий період або другий ряд зверху).
1 Знайдіть елемент в періодичній таблиці. Як приклад ми будемо розглядати ізотоп вуглецю 14С. Оскільки неізотопних вуглець 14С є просто вуглець С, знайдіть вуглець в періодичній таблиці (другий період або другий ряд зверху). 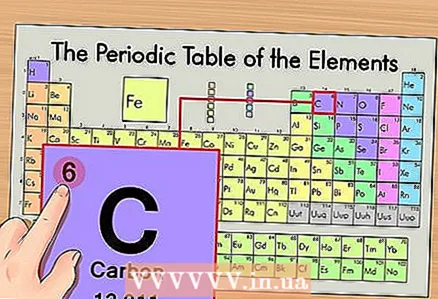 2 Знайдіть атомний номер елемента. Це, як правило, найбільш помітне число в комірці елемента і зазвичай знаходиться над його символом (в варіанті періодичної системи, яку ми використовуємо в нашому прикладі, інших номерів і немає). Атомний номер - це кількість протонів в одному атомі цього елементу. Вуглець знаходиться під номером 6, тобто один атом вуглецю має шість протонів.
2 Знайдіть атомний номер елемента. Це, як правило, найбільш помітне число в комірці елемента і зазвичай знаходиться над його символом (в варіанті періодичної системи, яку ми використовуємо в нашому прикладі, інших номерів і немає). Атомний номер - це кількість протонів в одному атомі цього елементу. Вуглець знаходиться під номером 6, тобто один атом вуглецю має шість протонів. 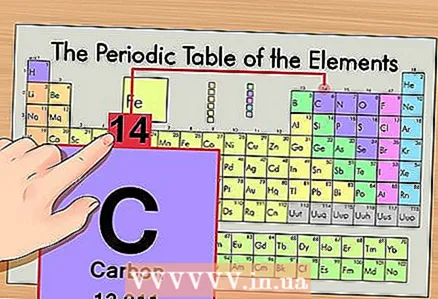 3 Знайдіть атомну масу. У разі ізотопів робити це дуже просто, так як вони названі відповідно до їх атомною масою. У нашому випадку у вуглецю 14С атомна маса дорівнює 14. Тепер ми знаємо атомну масу ізотопу; подальший процес розрахунку такої ж, як і для визначення числа нейтронів в атомах (НЕ ізотопи).
3 Знайдіть атомну масу. У разі ізотопів робити це дуже просто, так як вони названі відповідно до їх атомною масою. У нашому випадку у вуглецю 14С атомна маса дорівнює 14. Тепер ми знаємо атомну масу ізотопу; подальший процес розрахунку такої ж, як і для визначення числа нейтронів в атомах (НЕ ізотопи).  4 Відніміть атомний номер з атомної маси. Оскільки абсолютна частина атомної маси припадає на протони і нейтрони, віднімання числа протонів (тобто атомного номера, який дорівнює числу протонів) з атомної маси дає число нейтронів в атомі. У нашому прикладі: 14 (атомна маса) - 6 (число протонів) = 8 (число нейтронів).
4 Відніміть атомний номер з атомної маси. Оскільки абсолютна частина атомної маси припадає на протони і нейтрони, віднімання числа протонів (тобто атомного номера, який дорівнює числу протонів) з атомної маси дає число нейтронів в атомі. У нашому прикладі: 14 (атомна маса) - 6 (число протонів) = 8 (число нейтронів). 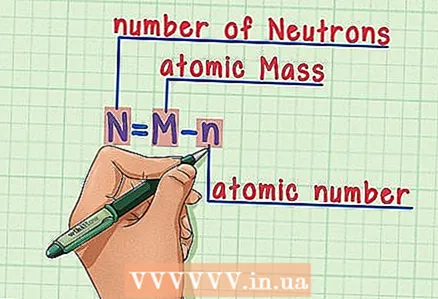 5 Запам'ятайте формулу. Щоб знайти число нейтронів в майбутньому, просто використовуйте цю формулу:
5 Запам'ятайте формулу. Щоб знайти число нейтронів в майбутньому, просто використовуйте цю формулу: - N = M - n
- N = кількість нейтронів
- M = атомна маса
- n = атомний номер
- N = M - n
Поради
- Протони і нейтрони становлять практично абсолютну масу елементів, в той час як електрони і інші частинки складають вкрай незначну масу (ця маса прагне до нуля).Так як один протон має приблизно ту ж масу, що і один нейтрон, а атомне число являє собою число протонів, то можна просто відняти число протонів від загальної маси.
- Осмій - метал в твердому стані при кімнатній температурі, отримав свою назву від грецького слова «osme» - запах.
- Якщо ви не впевнені, що означає якесь число в періодичній таблиці, запам'ятайте: таблиця, як правило, будується навколо атомного номера (тобто числа протонів), який починається з 1 (водень) і зростає на одну одиницю зліва направо, закінчуючись на 118 (Оганесон). Це тому, що число протонів в атомі визначає сам елемент і таке число - найбільш легкий спосіб систематизації елементів (наприклад, атом з 2 протонами - завжди гелій, так само, як і атом з 79 протонами - завжди золото).