Автор:
Lewis Jackson
Дата Створення:
5 Травень 2021
Дата Оновлення:
1 Липня 2024

Зміст
Моль - це стандартна одиниця виміру в хімії, яка використовується для розгляду різних елементів сполуки. Зазвичай маса сполуки обчислюється в грамах (г) і повинна бути перетворена в молярні одиниці. Перехід досить простий, однак, є ще кілька важливих кроків, яких нам потрібно виконати. Використовуючи метод нижче, ви можете легко перетворити грами в родимки.
Кроки
Частина 1 з 2: Обчисліть молекулярну масу
Підготуйте необхідні матеріали для вирішення математичної задачі. Коли у вас є всі доступні інструменти, вирішити проблему буде простіше. Що вам потрібно:
- Олівець і папір. Математика стає простішою, коли все записуєш на папері. Вам потрібно представити всі етапи для досягнення максимального балу.
- Періодична система хімічних елементів: використовується для визначення маси атомів елементів.
- Кишеньковий калькулятор: використовується для обчислення складних чисел.

Визначте, які елементи в сполуці потрібно перетворити в молярні одиниці. Першим кроком при розрахунку молекулярної маси є визначення елементів, що входять до складу сполуки. Це легко, оскільки абревіатура елементів складає лише один-два символи.- Якщо речовина скорочено двома літерами, перша буква буде написана великими літерами, а друга літера - малою. Приклад: Mg - це абревіатура елемента магній.
- Сполуки NaHCO3 складається з чотирьох елементів: натрію (Na), водню (H), вуглецю (C) та кисню (O).
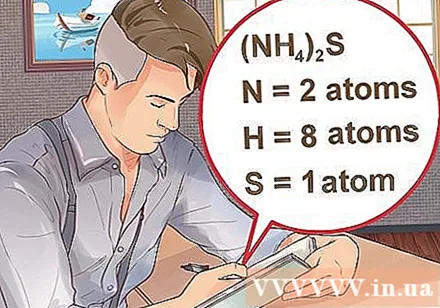
Визначте кількість атомів для кожного елемента сполуки. Вам потрібно знати атомний номер кожної речовини в сполуці, щоб розрахувати молекулярну масу цієї сполуки. Невелике число поряд із абревіатурою елемента представляє атомний номер елемента.- Приклад: з'єднання H2O має два атоми водню і один атом кисню.
- Якщо сполука записана в дужках, супроводжувана невеликим індексом, це означає, що кожен інгредієнт у дужках множить індекс. Приклад: з'єднання (NH4)2S складається з двох атомів N, восьми атомів H та одного атома S.

Запишіть кубічний атомний папір для кожного елемента. Використання періодичної системи - це найпростіший спосіб знайти кубічний атом елемента. Після того, як ви знайдете елемент у періодичній таблиці, ви побачите атомну масу безпосередньо під піктограмою елемента.- Наприклад, кубічний атом кисню дорівнює 15,99.
Обчисліть молекулярну масу. Масова молекула речовини дорівнює кількості атомів кожного елемента, помноженому на масовий атом цього елемента. Ця кількість необхідна для перетворення грама в моляр.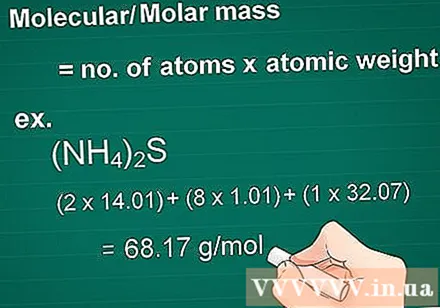
- Спочатку помножте атомний номер кожного елемента в сполуці на його масовий атом.
- Потім складіть маси елементів у складі.
- Приклад: Молекулярна маса сполуки (NH4)2S = (2 х 14,01) + (8 х 1,01) + (1 х 32,07) = 68,17 г / моль.
- Молекулярна маса також відома як молярна маса.
Частина 2 з 2: Перетворення грамів в моль
Налаштуйте формулу перетворення. Щоб знайти кількість молей сполуки, розділіть кількість грамів сполуки на молярну масу цієї сполуки.
- Формула: кількість молей = маса (грам) / молярна маса сполуки (грам / моль)
Підстави числа у формулу. Після налаштування правильної формули наступним кроком є заміна обчислених чисел на формулу. Якщо ви хочете переконатись, що дані знаходяться у правильному положенні, ви можете перевірити це, вимкнувши одиницю. Якщо після простоти залишилася одиниця - це родимки, тоді ви налаштовані правильно.
Розв’яжіть рівняння. За допомогою калькулятора розділіть масу на кубічну молекулу речовини або сполуки. Фактор буде кількістю молей речовини або сполуки, яку ви шукаєте.
- Наприклад, проблема полягає в 2 г води (H2O) і попросити вас перетворити його в молярні одиниці. Маємо молярну масу H2О дорівнює 18 г / моль. Поділіть 2 на 18, тож у вас вийде 0,1111 моль H2O.
Порада
- Не забудьте включити до відповідей назву елемента чи складової.
- Якщо вас попросять представити вправу або вікторину, обов’язково чітко покажіть свої відповіді, обвівши або намалювавши поле навколо відповідей.
Що тобі потрібно
- Хімічна періодична система
- Олівець
- Папір
- Комп’ютер
- Проблеми хімії